巧用活塞分离干燥混合气 CO₂与CO分离实验设计与试剂选择
分离和干燥一氧化碳(CO)与二氧化碳(CO₂)的混合气体,需要利用两者化学性质的显著差异。二氧化碳是酸性氧化物,能与碱液反应;而一氧化碳在常温下化学性质稳定,不与碱反应。因此,实验的核心是利用这一特性进行分离,再分别进行干燥以获得纯净气体。
一、 实验装置与操作流程概述
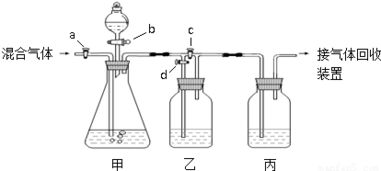
装置如图所示,包含四个可独立控制的活塞a、b、c、d,连接着气体通路和试剂储瓶。实验前所有活塞关闭。基本流程为:混合气体通入→吸收CO₂(分离)→分别干燥CO和富集CO₂的溶液→最终收集纯净、干燥的CO和CO₂气体。
二、 关键试剂选择与作用
- 吸收剂(用于分离CO₂):
- 首选试剂:浓氢氧化钠(NaOH)溶液。
* 作用原理:CO₂与NaOH反应生成碳酸钠(Na₂CO₃)或碳酸氢钠(NaHCO₃),从而被液体完全吸收。化学方程式为:
> 2NaOH + CO₂ → Na₂CO₃ + H₂O (CO₂量适中)
> NaOH + CO₂ → NaHCO₃ (CO₂过量)
- 优点:吸收效率极高,反应迅速、彻底,是实验室最常用的CO₂吸收剂。
- 替代选择:澄清石灰水[Ca(OH)₂溶液]。但其浓度低,吸收容量有限,且生成的碳酸钙(CaCO₃)微溶可能堵塞管路,故非最优选。
- 干燥剂(用于气体干燥):
- 对于分离出的CO气体:
- 首选试剂:浓硫酸(H₂SO₄) 或 无水氯化钙(CaCl₂)。
- 原理:二者均为中性或酸性干燥剂,具有强烈的吸水性,且不与CO发生任何反应。
- 对于从吸收液中释放出的CO₂气体:
- 释放CO₂:需向吸收了CO₂的NaOH溶液中加入强酸(如稀盐酸HCl或稀硫酸H₂SO₄),使碳酸盐分解释放出CO₂气体。
- 干燥CO₂:释放出的CO₂含有水蒸气,应使用浓硫酸(H₂SO₄)进行干燥。
- 注意:不能用碱性干燥剂(如碱石灰)干燥CO₂,因其会发生反应。
三、 实验步骤简述(配合活塞操作)
- 混合气体通入与CO₂吸收:打开活塞a和b,让混合气体缓慢通入盛有浓NaOH溶液的洗气瓶(或反应瓶)。CO₂被吸收,不含CO₂的CO气体(混有水蒸气)从出口导出。关闭a、b。
- CO的干燥与收集:将上述导出的湿润CO气体,通过打开活塞c,通入盛有浓硫酸的干燥瓶进行干燥,随后即可收集到纯净干燥的CO气体。操作完毕后关闭c。
- CO₂的释放与干燥:
- 关闭气体通路,打开活塞d,向已吸收CO₂的NaOH溶液中缓慢加入稀盐酸。此时会产生纯净的CO₂气体,但含有水蒸气及可能挥发出的少量HCl。
- 将此气体先通过一个盛有少量水或饱和NaHCO₃溶液的洗气瓶(图中可增设,或利用另一通路)以除去HCl,再通入浓硫酸干燥瓶中进行干燥。
- 最后收集纯净、干燥的CO₂气体。
四、
成功完成此实验的关键在于:
- 分离试剂:选择浓氢氧化钠溶液高效吸收CO₂。
- 干燥试剂:对两种气体均优先选用浓硫酸作为干燥剂。
- 释放试剂:使用稀盐酸从吸收液中重新获得CO₂。
- 活塞控制:通过精准控制活塞a、b、c、d的顺序开闭,实现气体的定向流动、试剂的分步加入,从而避免气体交叉污染,确保分离和干燥的彻底性。
此装置设计体现了在“液体分离及纯净设备制造”中,通过模块化阀门控制、针对不同物质性质选择特异性试剂,从而实现复杂混合物高效分离与提纯的核心思想。
如若转载,请注明出处:http://www.nydgyysyqhq.com/product/26.html
更新时间:2026-05-22 04:24:07